Konferencja Terapeutyczna Choroby Huntingtona 2017 – dzień 1
HDBuzz podsumowuje doniesienia z Konferencji Terapeutycznej Choroby Huntingtona 2017 na Malcie – dzień 1

Witajcie! To coroczna Konferencja Terapeutyczna Choroby Huntingtona na Malcie. Około 350 naukowców z całego świata pracujących nad HD zebrało się tutaj, aby przedyskutować najnowsze osiągnięcia w badaniach. Relacjonujemy na żywo za pośrednictwem Twittera i łączymy nasze doniesienia w codzienne artykuły.
Najważniejsze wiadomości ze zgromadzonych danych
Pierwszym mówcą jest Leslie Jones z Cardiff University, który bada, w jaki sposób genetyka wpływa na HD. Jones interesuje się tymi zmianami genetycznymi, które powodują, że u osób z mutacją HD objawy pojawiają się wcześniej lub później niż oczekiwano. Należy do konsorcjum badaczy „GeM-HD”, które w roku 2015 opublikowało przełomowe badanie. Różnice genetyczne, które zmieniają wiek pojawienia się objawów HD są podobne do tych, które stwierdzono u osób chorujących na inną chorobę degeneracyjną: „ataksję rdzeniowo-móżdżkową” (Spinocerebellar ataxia, SCA). Podobnie jak HD, niektóre formy SCA są spowodowane wydłużeniem fragmentu zawierającego powtórzenia „C-A-G” (w innych genach). Komórkom trudno prawidłowo kopiować te długie, powtarzające się odcinki „C-A-G”. W rezultacie długie powtórzenia CAG stają się coraz dłuższe, ze względu na omyłki w procesie kopiowania i naprawy DNA. Głównym wnioskiem badania GeM-HD jest to, że mutacje genów odpowiedzialnych za naprawę DNA wpływają na wiek pojawienia się objawów HD. Naukowcy pracujący nad HD nagle muszą się wiele nauczyć na temat procesu naprawy DNA!

Davina Hensman Moss (UCL) należy do grupy badającej, w jaki sposób różnice genetyczne wpływają na wiek pojawienia się objawów HD. Często mówimy o „początku objawów” HD, ale pojawiają się one stopniowo i powoli postępują przez długi czas. Wykorzystując dane z badania TRACK-HD Moss chce zrozumieć przebieg tego procesu. Informacje zgromadzone w badaniu TRACK-HD pozwoliły Moss stworzyć wyrafinowany komputerowy obraz progresji objawów HD. Potem postawiła bardzo mądre pytanie – czy ludzie, u których HD postępuje szybko (lub powoli), mają jakiekolwiek skorelowane różnice genetyczne? Poszukiwano zmian w całym genomie uczestników TRACK-HD, u których przebieg HD był nietypowy. Odkryto genetyczne odmiany poza genem HD, które prowadzą do zmiany szybkości postępowania objawów HD. Moss zauważa, że różnice w genach naprawy DNA zmieniają szybkość progresji HD. Potwierdza to, że proces naprawy DNA jest ważny w HD, choć szczegóły nie są jeszcze jasne. Jasne przesłanie płynące z tych badań jest takie, że pomaganie komórkom w dokładnym skopiowaniu powtórzeń CAG w genie HD jest niezwykle istotne. To odkrycie było możliwe wyłącznie dzięki tysiącom członków Społeczności HD biorących udział w badaniach i przekazujących swoje DNA. Te badania genetyczne wykonano przy użyciu technologii, która jeszcze nie istniała, gdy większość uczestników przekazywała DNA do badań.
Chris Kay (UBC) przemawia na konferencji na temat innego rodzaju odmian genetycznych – zmian w sekwencji genu HD poza regionem CAG. Kay odkrył wiele odmian, które występują znacznie częściej w genach HD z rozszerzeniami CAG. Pomaga to zrozumieć historyczne pochodzenie i światową ekspansję rozszerzeń CAG powodujących HD. Zapewnia również bardzo interesujące cele dla naukowców, którzy chcą selektywnie zmniejszyć poziom zmutowanego genu HD.
Christian Neri z firmy Inserm studiuje białko o nazwie FOXO i jego rolę w HD. FOXO pomaga komórkom mózgowym radzić sobie ze 'stresem’, naukowcy nazywają w ten sposób wszystko to, co utrudnia komórkom wykonywanie ich zadań. FOXO kontroluje wiele mechanizmów obronnych, które komórki mogą wykorzystać do przeżycia i poradzenia ze stresem.
Matthias Mann jest pionierem w dziedzinie „proteomiki”. Ta technologia umożliwia naukowcom dokładne mierzenie ilości tysięcy białek jednocześnie. Geny są ekscytujące, ale białka wykonują większość zadań komórki. Grupa Mann`a opracowała niezwykłe narzędzia do ich pomiaru. Mann i jego współpracownicy będą próbowali zastosować te narzędzia do śledzenia postępu HD.
„To odkrycie było możliwe wyłącznie dzięki tysiącom członków Społeczności HD biorących udział w badaniach i przekazujących swoje DNA.”
Wróg publiczny numer jeden: zmutowania huntingtyna
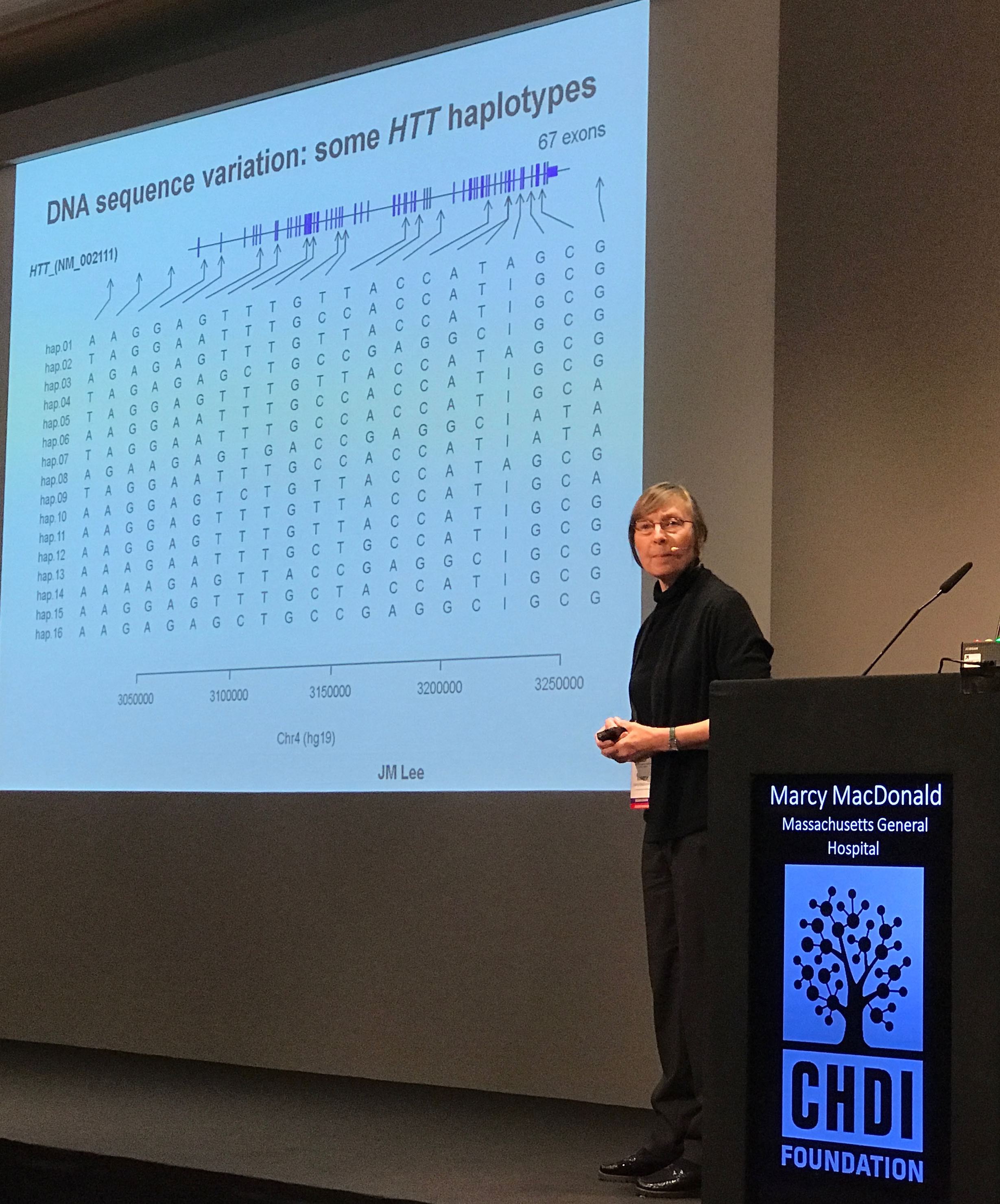
Marcy MacDonald (MGH) zajmowała się badaniem odmian genu HD. MacDonald jest kluczowym członkiem konsorcjum GeM-HD, które poszukuje odmian genu, wpływających na progresję objawów HD. Wykorzystując DNA ponad 7000 osób odkryto zupełnie nowy wariant, który wpływa na szybkość progresji objawów HD. Nowy wariant jest bardzo rzadki – tylko poprzez gromadzenie informacji od tysięcy wolontariuszy zespół był w stanie dokonać takiego odkrycia.
Darren Monckton (U. Glasgow) jest zainteresowany powtórzeniami CAG w genie HD. Od 1993 roku wiemy, że ekspansja powtórzeń CAG w genie HD jest przyczyną choroby. Od niedawna Monckton i inni badacze wiedzą, że powtórzenia CAG mogą wydłużyć się w czasie życia komórki. Zespół Moncktona wykorzystuje nowe techniki sekwencjonowania, aby szczegółowo zmierzyć długość ciągu powtórzeń CAG u 1000 pacjentów z HD. Mają nadzieję, że znalezienie rzadkich odchyleń w organizacji traktu CAG pomoże nam zrozumieć, w jaki sposób trakty CAG wydłużają się. Monckton stwierdził, że geny naprawy DNA, o których mówiła wcześniej dr Hensman Moss, wpływają na rozprzestrzenianie się powtórzeń CAG w komórce człowieka. (Pasek boczny: ilość CAG na wyniku testu genetycznego jest w rzeczywistości wartością przeciętną – różne komórki zawierają nieco inne ilości) Jedna z teorii tłumaczących, dlaczego niektóre przypadki HD postępują szybko jest taka, że ilość CAG we wrażliwych komórkach mózgowych może wzrosnąć. Genetycy nazywają to 'somatyczną niestabilnością’ powtórzeń CAG. Zrozumienie somatycznej niestabilności jest kluczową misją, ponieważ gdybyśmy mogli ją ograniczyć, moglibyśmy pomóc komórkom mózgu przetrwać dłużej. Zmniejszenie somatycznej niestabilności może również uniemożliwić wzrost liczby CAG w kolejnym pokoleniu.
Kevin Weeks (UNC) jest zainteresowany RNA – chemicznym pośrednikiem przenoszącym informacje z DNA do budowanych w komórkach białek. RNA jest często uważane za liniowy ciąg liter skopiowany z DNA, ale RNA fałduje się w złożone kształty o ważnych rolach. Laboratorium Weeks’a buduje naprawdę precyzyjne modele 3D kształtu RNA z genu HD. Kształt zmienia się wraz z liczbą powtórzeń CAG w genie HD – więcej CAG prowadzi do dużych zmian struktury 3D RNA. Te zmiany kształtu stanowią dla zespołu Weeks`a unikalny cel: namierzenie – a może zmniejszenie – ilości RNA zmutowanego genu. Otwiera to nowy sposób na powstrzymanie komórek od wytwarzania zmutowanej huntingtyny, najbardziej prawdopodobnego czynnika powodującego chorobę komórek w HD.
Podczas gdy HD najczęściej występuje w wieku dorosłym, Mark Mehler (Albert Einstein College of Medicine) koncentruje się na bardzo wczesnych zmianach. Odnajduje subtelne zmiany w rozwoju mózgu u myszy z bardzo długimi ekspansjami CAG w genie HD. Zmiany te mogą czynić komórki mózgu bardziej podatnymi w dojrzałym wieku.
Alberto Ruzo (Rockefeller) jest również zainteresowany procesem rozwojowym – procesem, w którym zapłodnione jajo staje się dorosłym osobnikiem. Podczas rozwoju specjalne komórki zwane „komórkami macierzystymi” dzielą się, aby ostatecznie wytworzyć wszystkie typy komórek znajdujących się w dorosłym ciele. Ruzo stworzył nowe komórki macierzyste, które są genetycznie identyczne, z wyjątkiem rosnącej liczby powtórzeń CAG w genie HD. Pozwala to badać proces, w wyniku którego dzielące się komórki macierzyste przybierają złożone kształty, co w efekcie prowadzi do powstania dorosłych narządów. Obserwują zmiany tych kształtów w komórkach z dłuższymi powtórzeniami CAG.
Więcej informacji o naszej polityce ujawniania informacji znajdziesz w naszym FAQ…