
Skaczące geny: białko choroby Huntingtona atakuje przeszczepy mózgowe
Długoterminowe badanie mózgów pacjentów z HD, którzy otrzymali przeszczepy tkanki płodowej, ujawnia zaskakujący wynik

Choroba Huntingtona jest spowodowana nieprawidłowym funkcjonowaniem i przedwczesną śmiercią komórek mózgowych. Zastąpienie tych martwych i umierających komórek komórkami macierzystymi od dawna jest celem niektórych naukowców zajmujących się HD. Nowe badanie analizuje długoterminowe zdrowie niektórych z najwcześniejszych przeszczepów komórkowych do mózgów pacjentów z HD — i odkrywa zaskakujący wynik.
Wypełnianie luk w mózgu z HD
Choroba Huntingtona i inne podobne choroby 'neurodegeneracyjne’ występują, gdy określone komórki w mózgu obumierają. Niestety dla osób noszących mutację HD, te kluczowe komórki mózgowe powstają głównie podczas wczesnego rozwoju. Po urodzeniu większość obszarów mózgu nie wytwarza wielu nowych komórek mózgowych, które zastąpiłyby te nieuchronnie tracone, nawet podczas normalnego starzenia się.
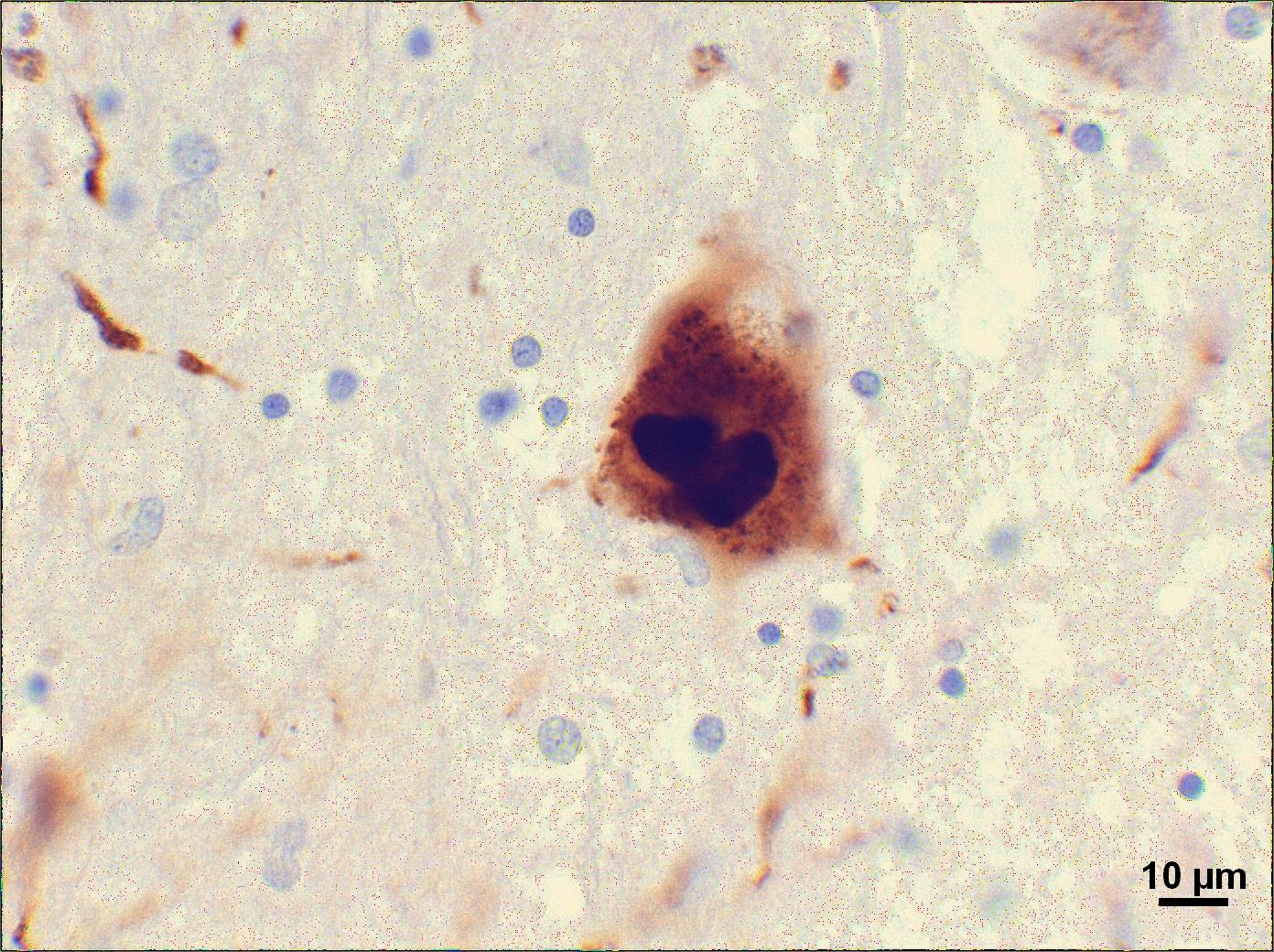
Źródło obrazu: Suraj Rajan
Co by było, gdybyśmy mogli pobrać tkankę z rozwijającego się mózgu i wykorzystać ją do wypełnienia ubytków w degenerującym się mózgu z HD? Chociaż może to brzmieć dość nieprzyjemnie, technicznie możliwe jest pobranie regionów mózgu z ludzkich embrionów i przeszczepienie ich do degenerujących się obszarów mózgu pacjentów z HD.
Terapia zastępowania komórek
W rzeczywistości, ta idea 'zastępowania komórek’ ma długą historię w HD. W połowie lat 80. seria badań na zwierzętach wykazała, że możliwe jest naprawienie uszkodzeń mózgu spowodowanych toksynami poprzez przeszczepienie embrionalnych komórek mózgowych do uszkodzonego obszaru. Późniejsze prace, na bardziej zaawansowanych modelach zwierzęcych, poparły ideę, że to podejście może być korzystne.
Na podstawie tych badań na zwierzętach i postępu podobnych prób w chorobie Parkinsona, niewielka liczba pacjentów z HD otrzymała przeszczepy embrionalnej tkanki mózgowej ponad 15 lat temu. Rozczarowująco, żaden z pacjentów otrzymujących przeszczepy nie wykazał znacznej ani trwałej poprawy objawów HD po otrzymaniu tych przeszczepów.
Jeden pacjent, który otrzymał przeszczep tkanki płodowej, zmarł około 18 miesięcy po operacji z przyczyn niezwiązanych z zabiegiem (choroba serca). Choć smutne dla pacjenta i jego rodziny, umożliwiło to naukowcom zbadanie przeszczepionej tkanki i sprawdzenie, jak radzi sobie w mózgu. Jednym z możliwych wyjaśnień, dlaczego pacjenci nie czuli się znacznie lepiej, jest to, że przeszczepy mogły nie przeżyć lub mogły nie nawiązać odpowiednich połączeń w mózgu gospodarza.
W rzeczywistości to wczesne badanie wykazało, że tkanka płodowa przeżyła w mózgu pacjenta z HD, a komórki w przeszczepie wydawały się nawiązywać takie połączenia, jakie powinny były nawiązać z innymi komórkami w mózgu. To dobra wiadomość, bo oznacza, że taki przeszczep jest technicznie możliwy, ale zła wiadomość, bo oznacza, że nie wiemy, dlaczego nie poprawił stanu pacjenta.
Nowe komórki, stare problemy
Po upływie większego czasu naukowcy byli w stanie zbadać większą liczbę mózgów pacjentów z chorobą Huntingtona, którzy ostatecznie zmarli z powodu HD, lata po otrzymaniu przeszczepów tkanki płodowej. Ta analiza wskazała na bardziej rozczarowujący powód niepowodzenia przeszczepionej tkanki w pomaganiu pacjentom z HD: nowe komórki wydawały się umierać, podobnie jak stare komórki wokół nich.
To było nieoczekiwane! Pamiętaj, że komórki przeszczepione do mózgów pacjentów z HD pochodziły z ludzkich embrionów, więc były bardzo młode. Mimo to coś w byciu wewnątrz mózgu z HD sprawiło, że te zupełnie nowe komórki zachorowały i faktycznie zaczęły umierać jak komórki, które miały zastąpić.
Podobne rozczarowujące wyniki zaobserwowano u pacjentów z chorobą Parkinsona, którzy otrzymali przeszczepy tkanki płodowej, co sugeruje, że może to być ogólny problem z całą ideą terapii zastępowania komórek. Może być tak, że mózgi pacjentów z neurodegeneracją są po prostu zbyt nieprzyjazne, żeby nowe komórki mogły być pomocne.
Koniec z sąsiedztwem
Ale jak to możliwe? Jeśli komórki dawcy nie mają mutacji HD, dlaczego chorują tak samo jak te komórki, które ją mają? Nie znamy jeszcze odpowiedzi na to pytanie, ale rosnąca liczba prac sugeruje, że komórki mózgowe u osób z neurodegeneracją mogą faktycznie wzajemnie się zarażać.
„Zespół Cicchettiego zauważył coś dziwnego w przeszczepionych tkankach płodowych w mózgach pacjentów z HD — zawierały one agregaty! To bardzo zaskakujące, ponieważ te przeszczepione tkanki nie mają zmutowanego genu HD.”
W wielu chorobach neurodegeneracyjnych komórki mózgowe są pełne skupisk śmieci. Te skupiska nazywane są 'agregatami’ w HD, 'ciałami Lewy’ego’ w chorobie Parkinsona i 'płytkami amyloidowymi’ w chorobie Alzheimera. W każdym przypadku komórki w pewnych obszarach mózgu wydają się niezdolne do usunięcia komórkowych śmieci, co może przyczyniać się do ich chorowania i obumierania.
Gdy przeszczepy płodowe zostały wszczepione do mózgów pacjentów z chorobą Parkinsona, odkryto, że komórki w przeszczepie zawierają ciałka Lewy’ego, tak jak chore komórki wokół nich. To było bardzo zaskakujące – to są zdrowe młode komórki, a normalnie rozwój choroby Parkinsona trwa dziesięciolecia.
Nowe prace nad HD
Czy coś podobnego może dziać się w przeszczepach choroby Huntingtona? Najnowsze badanie grupy naukowców kierowanej przez Francescę Cicchetti z Université Laval sugeruje, że może dziać się coś dziwnego. Cicchetti zbadała mózgi 3 pacjentów z HD, którzy zmarli około 10 lat po otrzymaniu przeszczepów tkanki płodowej.
Aby zrozumieć te odkrycia, musimy pamiętać o kilku rzeczach dotyczących działania HD. Każdy pacjent z HD odziedziczył zmutowaną kopię genu HD, która powoduje, że jego komórki wytwarzają zmutowane białko HD. To właśnie to zmutowane białko HD powoduje uszkodzenia w mózgu z HD. W rzeczywistości większość tych skupisk śmieci znalezionych w komórkach mózgowych HD (’agregaty’) składa się ze zmutowanego białka HD.
Zespół Cicchetti zauważył coś dziwnego w przeszczepionej tkance płodowej w mózgach pacjentów z HD — zawierała agregaty! To bardzo zaskakujące, bo ta przeszczepiona tkanka nie ma zmutowanego genu HD, więc nie powinna mieć w sobie żadnego zmutowanego białka HD. Co się dzieje?
Żeby było jasne: skupiska zmutowanego białka HD nie są wewnątrz komórek przeszczepu, ale raczej przyklejone na zewnątrz komórek jak śmieci, których tam nie powinno być. Wyjaśnienie tego zaskakującego wyniku nie jest jasne, ale ustalenie, skąd pochodzą te skupiska i czy przyczyniają się do niepowodzenia tych przeszczepów, będzie ważnym obszarem pracy. Ale przynajmniej teraz wiemy, że tam są.
Więc co teraz?
Wyniki tego badania, jak również innych badań w innych chorobach neurodegeneracyjnych, sugerują, że musimy być bardzo ostrożni z prostym zastępowaniem martwych komórek w degenerującym mózgu. Jeśli podstawowa choroba nadal jest obecna, nowe komórki, które umieścimy w mózgu, mogą po prostu również zachorować.
To nieco rozczarowująca wiadomość w kontekście osiągnięcia terapii zastępowania komórek dla HD. Ale wielkie postępy są dokonywane w nauce o komórkach macierzystych w laboratoriach na całym świecie, więc ta historia nie jest końcem tej konkretnej drogi. Wreszcie, choć zastępowanie komórek to atrakcyjny pomysł, prace nad zwiększeniem przeżywalności komórek mózgowych, zamiast zastępowania ich po śmierci, szybko się rozwijają i trwają pełną parą.
Dowiedz się więcej
Więcej informacji o naszej polityce ujawniania informacji znajdziesz w naszym FAQ…


